Klant login
Log in
Registreer
Het aanmaken van een account heeft vele voordelen:
- Bekijk bestelling en verzendstatus
- Bekijk bestelgeschiedenis
- Reken sneller af
Winkelwagen
Subtotaal winkelwagen
U heeft geen product(en) in uw winkelwagen.
Talen
Google Translate:
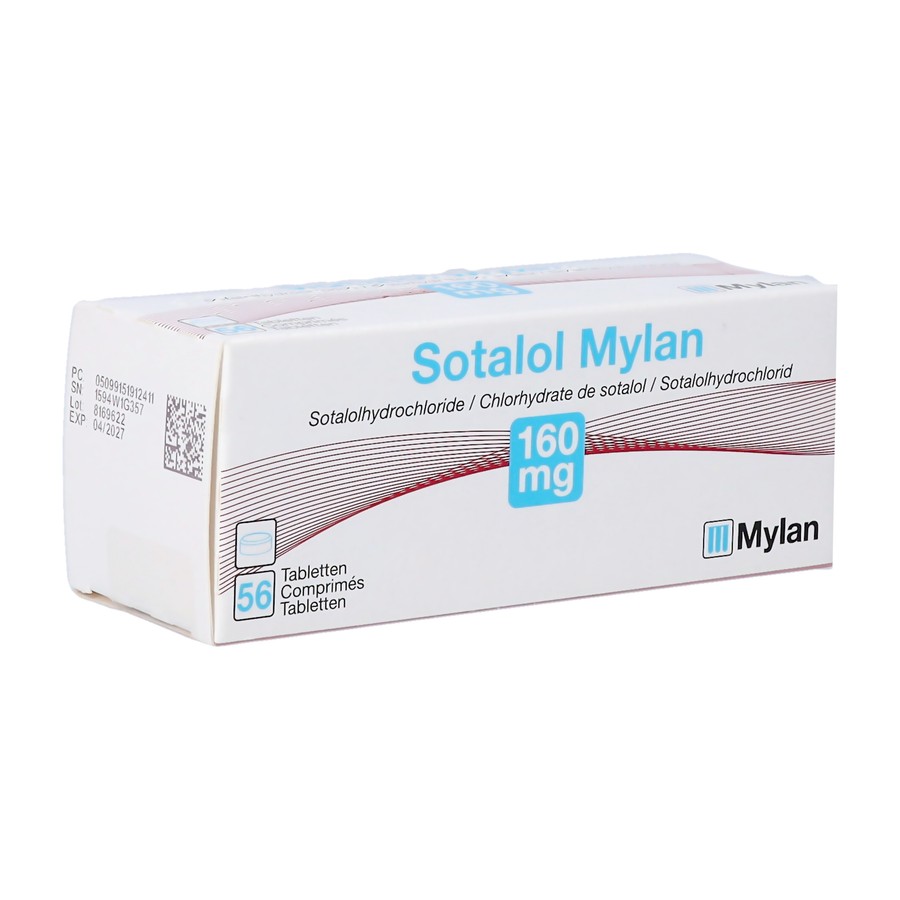
Sotalol Viatris 160mg Tabl 56
Terugbetaalbaar
Als je recht hebt op een terugbetaling voor dit geneesmiddel, betaal je in de apotheek een verlaagde prijs en niet de prijs die op onze webshop vermeld staat.
Terugbetalingstarief
€ 2,00 (6% inclusief btw)
Verhoogde tegemoetkoming
€ 1,00 (6% inclusief btw)
Dit product moet worden goedgekeurd door de apotheker.
Belangrijke informatie
Voor dit geneesmiddel is een voorschrift nodig. Na beoordeling door de apotheker kan je het komen afhalen en betalen in de apotheek.
Maximum toegelaten hoeveelheid in winkelwagen bereikt
Op bestelling
4.4 Bijzondere waarschuwingen en voorzorgen bij gebruik Plotse stopzetting: overgevoeligheid voor catecholamines is waargenomen bij patiënten bij wie de behandeling met een bètablokker wordt stopgezet. Er zijn zeldzame gevallen gemeld van verergering van angina pectoris, aritmie en in sommige gevallen myocardinfarct als een behandeling met een bètablokker plots werd stopgezet. Patiënten moeten zorgvuldig worden gevolgd als een chronische behandeling met sotalol wordt stopgezet, vooral als ze ischemisch hartlijden vertonen. Indien mogelijk moet de dosis geleidelijk worden afgebouwd over een periode van één tot twee weken. Aangezien aandoeningen van de coronaire arteriën vaak voorkomen en mogelijk niet worden ontdekt bij patiënten die sotalol krijgen, kan plotse stopzetting bij patiënten met aritmie latente coronaire insufficiëntie demaskeren. Bovendien kan hypertensie optreden. Proaritmie: de gevaarlijkste bijwerking van antiaritmica van klasse III is de verergering van een vooraf bestaande aritmie of de uitlokking van een nieuwe aritmie. Geneesmiddelen die het QT-interval verlengen kunnen torsade de pointes veroorzaken, een polymorfe ventriculaire tachycardie geassocieerd met een verlenging van het QT-interval. De ervaring tot dusver wijst erop dat er een verband bestaat tussen het risico op torsade de pointes en verlenging van het QT-interval, daling van de hartslag, daling van het serumkalium en –magnesium (bijvoorbeeld als gevolg van diureticagebruik), hoge sotalolconcentraties in het plasma (bijvoorbeeld als gevolg van overdosering of nierinsufficiëntie) en het gelijktijdig gebruik van sotalol en andere geneesmiddelen zoals antidepressiva en klasse I-antiaritmica die in verband worden gebracht met torsade de pointes (zie rubriek 4.5). Vrouwen kunnen een hoger risico lopen om torsade de pointes te ontwikkelen. Ecg-monitoring onmiddellijk voor of na de episodes toont meestal een significante verlenging van het QT-interval en een significante verlenging van het QTc-interval aan. In klinische studies werd sotalol over het algemeen niet toegediend aan patiënten die voor de behandeling een QTc-interval van meer dan 450 msec hadden. De dosis van sotalol moet zeer voorzichtig worden opgevoerd bij patiënten met een verlenging van het QT-interval. De incidentie van torsade de pointes is dosisafhankelijk. Torsade de pointes treedt meestal op binnen 7 dagen na het begin van de behandeling of de dosisverhoging, en verdwijnt bij de meeste patiënten spontaan. Hoewel de meeste episodes van torsade de pointes zelfbeperkend zijn of gepaard gaan met symptomen (bv. syncope), kunnen ze uitmonden in ventrikelfibrillatie. Klinische studies naar artimie: tijdens klinische studies heeft 4,3% van de 3.257 patiënten met aritmie een nieuwe of verergerde ventrikelaritmie vertoond, met inbegrip van aanhoudende ventriculaire tachycardie (ongeveer 1%), en torsade de pointes (2,4%). Daarnaast werden sterfgevallen bij ongeveer 1% van de patiënten beschouwd als mogelijk gerelateerd aan het geneesmiddel. Bij patiënten met andere, minder ernstige ventriculaire en supraventriculaire aritmieën bedroeg de incidentie van torsade de pointes respectievelijk 1% en 1,4%. Zoals hieronder aangegeven waren ernstige gevallen van proaritmie, met inbegrip van torsade de pointes dosisafhankelijk: Percentuele incidentie van ernstige proaritmie* per dosis bij patiënten met aanhoudende VT/VF dagdosis (mg) Incidentie van ernstige proaritmie* Patiënten (n) 1-80 0 (0/72) 81-160 0,5% (4/838) 161-320 1,8% (17/960) 321-480 4,5% (21/471) 481-640 4,6% (15/327) > 640 6,8% (7/103) *Torsade de pointes of nieuwe aanhoudende VT/VF In klinische studies bij patiënten met aanhoudende VT/VF was de incidentie van ernstige proaritmie (torsade de pointes of nieuwe aanhoudende VT/VF) <2% bij dosissen tot 320 mg. Bij hogere dosissen steeg de incidentie met meer dan factor 2. Andere risicofactoren voor torsade de pointes waren een te sterke verlenging van het QTc en een voorgeschiedenis van cardiomegalie of congestief hartfalen. Patiënten met aanhoudende ventriculaire tachycardie en een voorgeschiedenis van congestief hartfalen lopen het hoogste risico op ernstige proaritmie (7%). Er moet niet alleen rekening worden gehouden met de mogelijkheid van proaritmische effecten bij de start van de behandeling, maar ook bij elke verhoging van de dosis. Die effecten treden meestal binnen 7 dagen na de start van de behandeling of na een dosisverhoging op. Het risico op proaritmie is kleiner als de behandeling wordt gestart met 80 mg en als die dosis daarna geleidelijk wordt verhoogd. Voorzichtigheid is geboden bij patiënten die al sotalol krijgen als het QTc onder behandeling langer is dan 500 msec, en er moet ernstig worden overwogen om de dosis te verlagen of de behandeling stop te zetten als het QTc-interval langer is dan 550 msec. Aangezien er meerdere risicofactoren bestaan voor torsade de pointes, is voorzichtigheid echter geboden ongeacht de lengte van het QTc-interval. Elektrolytenstoornissen: Sotalol Viatris mag pas worden gebruikt bij patiënten met hypokaliëmie of hypomagnesiëmie na correctie van die afwijkingen; die stoornissen kunnen de mate van QT-verlenging versterken en het risico op torsade de pointes verhogen. Er moet speciaal aandacht worden besteed aan het elektrolyten- en zuur�base-evenwicht bij patiënten met ernstige of langdurige diarree of patiënten die tegelijkertijd magnesium- en/of kaliumafdrijvende middelen krijgen. Congestief hartfalen: bètablokkers kunnen de contractiliteit van het myocard verder verminderen en ernstiger hartfalen uitlokken. Voorzichtigheid is geboden als een behandeling wordt gestart bij patiënten met een gestoorde linkerventrikelfunctie die onder controle is met een behandeling (bv. ACE-remmers, diuretica, digitalis, enz%); een lagere startdosis en voorzichtige verhoging van de dosering krijgen dan de voorkeur. Recent MI: bij patiënten met een voorgeschiedenis van infarct en gestoorde linkerventrikelfunctie, moeten de risico's van toediening van sotalol worden afgewogen tegen de voordelen ervan. Een zorgvuldige monitoring en verhoging van de dosis zijn cruciaal in het begin en bij de follow-up van de behandeling. De ongunstige resultaten van klinische studies met antiaritmica (namelijk een aantoonbare verhoging van de mortaliteit), wijzen erop dat Sotalol Viatris moet worden vermeden bij patiënten met een linkerventrikelejectiefractie <40% die geen ernstige ventriculaire aritmie vertonen. Elektrocardiografische veranderingen: te sterke verlenging van het QT-interval, >550 msec, kan een teken zijn van toxiciteit en moet worden vermeden (zie hoger onder proaritmie). Sinusbradycardie werd zeer vaak gezien bij patiënten met aritmie die sotalol kregen in klinische studies. Bradycardie verhoogt het risico op torsade de pointes. Sinuspauze, sinusarrest en sinusknoopdysfunctie treden op bij minder dan 1% van de patiënten. De incidentie van 2e- of 3e-graads AV-blok is ongeveer 1%. Anafylaxie: patiënten met een anafylactische reactie op meerdere allergenen in de voorgeschiedenis kunnen een ernstigere reactie vertonen bij een nieuwe blootstelling als ze bètablokkers innemen. Patiënten met een voorgeschiedenis van ernstige overgevoeligheidsreacties en patiënten die momenteel een desensibilisatiebehandeling ondergaan, lopen een hoger risico op ontwikkeling van excessieve anafylactische reacties. Sotalolhydrochloride mag daarom uitsluitend aan deze patiënten worden toegediend als dat absoluut geïndiceerd is. Dergelijke patiënten reageren soms niet op de gebruikelijke doses adrenaline die worden gebruikt om een allergische reactie te behandelen. Anesthesie: net zoals met andere bètablokkers is voorzichtigheid geboden als Sotalol Viatris wordt gebruikt bij patiënten die een heelkundige ingreep ondergaan en in combinatie met anesthetica die de werking van het myocard onderdrukken, zoals cyclopropaan of trichloorethyleen. Sotalol mag voorzichtig worden toegediend aan patiënten met obstructieve aandoeningen van de luchtwegen op voorwaarde dat ze voldoende gecontroleerd worden. Als de weerstand van de luchtwegen toeneemt, moet overwogen worden om de bètablokker stop te zetten, afhankelijk van de mate van weerstand in de luchtwegen en de voordelen van de bètablokkerende werking. Diabetes Mellitus: Sotalol Viatris moet voorzichtig worden gebruikt bij patiënten met diabetes (vooral als de diabetes niet goed gereguleerd is) of met episodes van spontane hypoglycemie in de voorgeschiedenis, aangezien bètablokkade een aantal belangrijke tekenen van een beginnende acute hypoglycemie zoals tachycardie kan maskeren. Thyreotoxicose: bètablokkade kan bepaalde klinische tekenen van hyperthyreoïdie maskeren (bv. tachycardie). Patiënten van wie wordt vermoed dat ze thyreotoxicose ontwikkelen, moeten zorgvuldig worden behandeld om abrupte stopzetting van de bètablokkade te vermijdenDie kan de symptomen van hyperthyreoïdie, waaronder thyroïdstorm, immers verergeren. Leverinsufficiëntie: aangezien sotalol geen eerstepassagemechanisme ondergaat, verandert de klaring van sotalol niet bij patiënten met leverinsufficiëntie. Nierinsufficiëntie: sotalol wordt vooral via de nieren uitgescheiden via glomerulaire filtratie en in beperkte mate via tubulaire secretie. Er bestaat evenwel een direct verband tussen de nierfunctie, gemeten op basis van het serumcreatinine of de creatinineklaring, en de eliminatiehalfwaardetijd van sotalol en de urinaire excretie daarvan. De dosis moet worden aangepast bij patiënten met een gestoorde nierfunctie (zie rubriek 4.2). Feochromocytoom: sotalolhydrochloride mag niet worden toegediend aan patiënten met een feochromocytoom tenzij ze gelijktijdig behandeld worden met een alfablokker. Psoriasis: er zijn zeldzame gevallen gemeld van verergering van de symptomen van psoriasis vulgaris door bètablokkers.
- Profylaxe en controle van de frequentie van flutter en auriculaire fibrillatie
- Onderdrukking van levensbedreigende ventriculaire tachycardie en preventie van induceerbare ventriculaire tachycardie
Welke stoffen zitten er in dit middel?
De werkzame stof in dit middel is sotalolhydrochloride. De tablet van 160 mg bevat 160 mg sotalolhydrochloride.
De andere stoffen in dit middel zijn: calciumwaterstoffosfaat, maiszetmeel, povidon, natriumzetmeelglycolaat, talk en magnesiumstearaat.
Neem Sotalol Viatris niet samen in met:
andere geneesmiddelen tegen hartritmestoornissen (bv. verapamil, kinidine, diltiazem, disopyramide, procaïnamide, flecaïnide, amiodaron, bepridil) andere bètablokkers (geneesmiddelen die worden gebruikt tegen angina, hoge bloeddruk of preventie van migraine)
Het is vooral belangrijk dat u uw arts inlicht als u één van de volgende geneesmiddelen inneemt:
geneesmiddelen gebruikt om diabetes te behandelen (bv. metformine of insuline) geneesmiddelen gebruikt om astma en andere longziekten te behandelen (bv. salbutamol, terbutaline of isoprenaline via inhalatie) geneesmiddelen gebruikt om depressie (bv. imipramine, maprotiline), angst, zenuwaandoeningen en psychische stoornissen (bv. haloperidol) te behandelen geneesmiddelen gebruikt om allergie zoals hooikoorts te behandelen (bepaalde antihistaminica zoals astemizol en terfenadine) plastabletten (diuretica) geneesmiddelen die worden gebruikt bij hoge bloeddruk of het raynaudfenomeen (bv. amlodipine, nifedipine) methyldopa, reserpine of quanethidine (geneesmiddelen die worden gebruikt om de bloeddruk te reguleren) geneesmiddelen die worden gebruikt om hartfalen te behandelen (bv. digoxine) het geneesmiddel halofantrine (gebruikt om malaria te behandelen) bepaalde antibiotica (vb. pentamidine en floxacine-antibiotica zoals ciprofloxacine)
Of als u de volgende geneesmiddelen inneemt:
clonidine (soms gebruikt om warmteopwellingen of hoofdpijn te behandelen). Als u tijdens de behandeling met clonidine en sotalol moet stoppen, moet u eerst stoppen met sotalol door de dosis traag af te bouwen voor u met clonidine stopt. steroïden laxeermiddelen het geneesmiddel floctafenine (gebruikt tegen pijn en ontsteking) het geneesmiddel amfotericine B (gebruikt tegen schimmelinfecties)
Zoals elk geneesmiddel kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Ernstige bijwerkingen
Licht uw arts onmiddellijk in of ga naar het dichtstbijzijnde ziekenhuis als u een van de volgende symptomen krijgt: zwelling van het gezicht, de lippen, de tong en/of de keel met slik- of ademhalingsproblemen. Dat kunnen tekenen zijn van een allergische reactie en de tabletten zullen worden stopgezet.
Niet bekend (frequentie kan met de beschikbare gegevens niet worden bepaald):
• hartstilstand (veroorzaakt plotse collaps, geen pols, geen ademhaling en verlies van het bewustzijn)
Andere mogelijke bijwerkingen
Vaak (kunnen optreden bij tot 1 op de 10 mensen):
• onregelmatige hartslag, trage hartslag, pijn op de borst, lage bloeddruk, ademhalingsproblemen, zwelling, flauwvallen en hartkloppingen, veranderingen van het hartritme (torsade de pointes, verlengd QT-interval, AV-geleidingsstoornis, ventrikeltachycardie), verergering van angina pectoris (veroorzaakt pijn op de borst)
• verergering van perifere occlusieve ziekte, koude ledematen
• misselijkheid en braken, indigestie, buikpijn, winderigheid, diarree, krampen
• angst, depressie, verwardheid, stemmingsveranderingen, hoofdpijn, ijlhoofdigheid, duizeligheid, algemene zwakte, vermoeidheid, slaapproblemen, tintelingen in de voeten en de handen
• seksuele disfunctie, impotentie, koorts, uitslag, huidreacties, gehoorproblemen, gezichtsproblemen, smaakveranderingen
Niet bekend (frequentie kan met de beschikbare gegevens niet worden bepaald):
• Te weinig bloedplaatjes in het bloed. (Trombocytopenie) Bloedplaatjes zorgen voor korstjes op een wond. Als u te weinig bloedplaatjes heeft, kunt u last hebben van blauwe plekken, rode puntjes op de huid, een bloedneus of wondjes die langer blijven bloeden
• hallucinaties, abnormale dromen
• wazig zicht, conjunctivitis, ontsteking van het hoornvlies (keratoconjunctivitis), verminderde traansecretie (vooral bij dragers van contactlenzen)
• droge mond
• psoriasis (huidziekte) kan worden uitgelokt of kan verergeren, haaruitval, overmatig zweten
• stijging van vetten en daling van suiker in het bloed
Patiënten die dit soort geneesmiddel innamen, hebben ook geklaagd over koude en/of blauwe vingers en tenen, verergering van pijn in de benen bij het lopen, huiduitslag of droge ogen.
Het melden van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker. Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via:
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
Afdeling Vigilantie
Postbus 97
1000 Brussel
Madou
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg.be
Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Wanneer mag u dit middel niet gebruiken?
als u allergisch bent voor één van stoffen in dit geneesmiddel. Deze stoffen kunt u
vinden in rubriek 6.
als u last heeft van astma, aanvallen van piepende ademhaling of een andere
longaandoening
als u een heel trage hartslag of een heel lage bloeddruk heeft
als u een aandoening heeft die verkleuring (wit of purper) van de handen en de voeten
veroorzaakt (syndroom van Raynaud)
als u een ernstige circulatiestoornis heeft
als u een hartaandoening heeft gehad (zoals onbehandeld hartfalen, hartblok,
ziekesinussyndroomof een cardiogene shock
als u een aandoening heeft die metabole acidose wordt genoemd
als u een onbehandelde tumor heeft van de bijnier (zie rubriek 'Wanneer moet u extra
voorzichtig zijn met dit middel?')
als u nierfalen vertoont
als u geopereerd moet worden en een verdovingsmiddel nodig heeft, vertel uw
anesthesist of tandarts dan dat u Sotalol Viatris inneemt
als u intraveneus verapamil of diltiazem gebruikt (geneesmiddelen om een
onregelmatige hartslag te behandelen)
Bijsluiter
3/9
Als een van bovenstaande omstandigheden op u van toepassing is, moet u met uw arts
spreken voor u dit geneesmiddel inneemt.
4.6 Vruchtbaarheid, zwangerschap en borstvoeding Zwangerschap Dierstudies met sotalol hydrochloride wezen niet op teratogeniciteit of andere schadelijke effecten op de foetus. Hoewel er geen afdoende en goed gecontroleerde studies zijn uitgevoerd bij zwangere vrouwen, is aangetoond dat sotalol hydrochloride door de placenta gaat en aanwezig is in het amnionvocht. Bètablokkers zorgen voor een vermindering van de placentaire doorbloeding hetgeen kan resulteren in intra�uteriene vruchtdood, en immature of premature bevalling. Bovendien kunnen er bijwerkingen (met name hypoglycemie en bradycardie) optreden bij de foetus en de neonatus. Er bestaat een verhoogd risico op cardiale en pulmonale complicaties bij de neonatus in de postnatale periode. Daarom mag Sotalol Viatris tijdens de zwangerschap alleen worden gebruikt als de mogelijke voordelen opwegen tegen het risico voor de foetus. Sotalol moet 48 – 72 uur voor de verwachte bevalling worden stopgezet. Als dat niet mogelijk is, moet de pasgeborene tot 48 – 72 uur na de geboorte gecontroleerd worden op tekenen en symptomen van bètablokkering (vb. hart- en longcomplicaties). Borstvoeding De meeste bètablokkers en vooral de lipofiele verbindingen gaan over in de moedermelk, hoewel in wisselende mate. Daarom wordt borstvoeding niet aanbevolen tijdens een behandeling met dergelijke verbindingen. Als sotalolhydrochloride tijdens de periode van borstvoeding wordt gebruikt, dienen de baby's te worden gecontroleerd op tekenen van een bètablokkade. Vruchtbaarheid Er zijn geen klinische gegevens beschikbaar over de vruchtbaarheid bij gebruik van dit geneesmiddel. Er zijn gegevens beschikbaar over de vruchtbaarheid bij dieren.
Aritmie
- Begindosis: 80 mg 1 - 2 x /dag
- Onderhoudsdosis: 160 mg 2 x /dag
- Max. dosis: 640 mg /dag
- Dosistitratie langzaam onder strikt medisch toezicht en ECGcontrole
- Dosisaanpassingen zijn aangewezen bij nierinsufficiëntie
| CNK | 1560929 |
|---|---|
| Organisaties | Viatris |
| Merken | Viatris |
| Breedte | 53 mm |
| Lengte | 128 mm |
| Diepte | 26 mm |
| Hoeveelheid verpakking | 56 |
| Actieve ingrediënten | sotalol hydrochloride |
| Behoud | Kamertemperatuur (15°C - 25°C) |