Klant login
Log in
Registreer
Het aanmaken van een account heeft vele voordelen:
- Bekijk bestelling en verzendstatus
- Bekijk bestelgeschiedenis
- Reken sneller af
Winkelwagen
Subtotaal winkelwagen
U heeft geen product(en) in uw winkelwagen.
Talen
Google Translate:
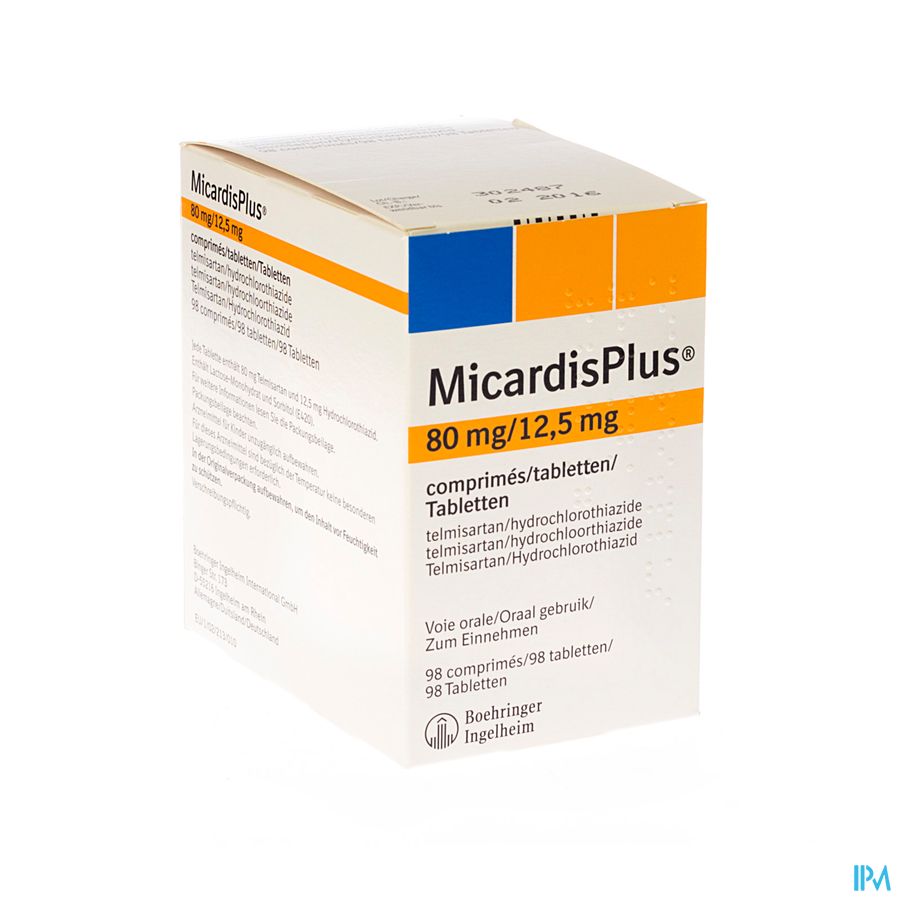
Micardisplus Comp 98 X 80mg/12,5mg
Terugbetaalbaar
Als je recht hebt op een terugbetaling voor dit geneesmiddel, betaal je in de apotheek een verlaagde prijs en niet de prijs die op onze webshop vermeld staat.
Terugbetalingstarief
€ 7,38 (6% inclusief btw)
Verhoogde tegemoetkoming
€ 4,38 (6% inclusief btw)
Belangrijke informatie
Voor dit geneesmiddel is een voorschrift nodig. Na beoordeling door de apotheker kan je het komen afhalen en betalen in de apotheek.
Niet beschikbaar
Neem contact op met ons via telefoon of e-mail, dan bekijken we samen de mogelijkheden.
4.4 Bijzondere waarschuwingen en voorzorgen bij gebruik Zwangerschap Therapie met angiotensine II-receptorblokkers mag niet gestart worden tijdens de zwangerschap. Patiënten die een zwangerschap plannen, moeten omgezet worden op een alternatieve antihypertensieve therapie met een bekend veiligheidsprofiel voor gebruik tijdens de zwangerschap, tenzij het voortzetten van de angiotensine II-receptorblokkertherapie noodzakelijk wordt geacht. Als zwangerschap wordt vastgesteld, dient de behandeling met angiotensine II-receptorblokkers onmiddellijk te worden gestaakt, en moet, indien nodig, met een alternatieve therapie begonnen worden (zie rubriek 4.3 en 4.6). Leverinsufficiëntie Telmisartan/HCTZ mag niet worden gegeven aan patiënten met cholestasis, galwegobstructies of ernstige leverinsufficiëntie (zie rubriek 4.3) aangezien telmisartan grotendeels met de gal wordt uitgescheiden. Het is te verwachten dat deze patiënten een lagere hepatische klaring voor telmisartan hebben. Daarnaast dient telmisartan/HCTZ met voorzichtigheid te worden gebruikt bij patiënten met een verminderde leverfunctie of een progressieve leveraandoening, aangezien kleine veranderingen in de vocht- en elektrolytenbalans een hepatisch coma kunnen veroorzaken. Er is geen klinische ervaring met telmisartan/HCTZ bij patiënten met leverinsufficiëntie. Renovasculaire hypertensie Er bestaat een verhoogd risico op ernstige hypotensie en nierinsufficiëntie wanneer patiënten met bilaterale nierarteriestenose of stenose van de arterie van een enkele functionerende nier behandeld worden met geneesmiddelen die het renine-angiotensine-aldosteronsysteem beïnvloeden. Nierinsufficiëntie en niertransplantatie Telmisartan/HCTZ mag niet worden gebruikt door patiënten met ernstige nierinsufficiëntie (creatinineklaring < 30 ml/min) (zie rubriek 4.3). Er is geen ervaring met het toedienen van telmisartan/HCTZ bij patiënten met een recente niertransplantatie. De ervaring met telmisartan/HCTZ bij patiënten met milde tot matige nierinsufficiëntie is beperkt, en daarom wordt periodieke controle van kalium-, creatinine- en urinezuurserumspiegels aanbevolen. Thiazidediureticageassocieerde azotemie kan voorkomen bij patiënten met nierinsufficiëntie. Telmisartan wordt niet uit het bloed verwijderd door hemofiltratie en is niet dialyseerbaar. Patiënten met volume- en/of natriumdepletie Symptomatische hypotensie, vooral na de eerste dosering, kan voorkomen bij patiënten die een volume- en/of natriumdepletie hebben door therapie met een sterk werkzaam diureticum, een zoutarm dieet, diarree of braken. Dergelijke situaties, in het bijzonder volume- en/of natriumdepletie, dienen vóór toediening van MicardisPlus gecorrigeerd te worden. Er zijn uitzonderlijke gevallen van hyponatriëmie, die gepaard gingen met neurologische symptomen (misselijkheid, progressieve desoriëntatie, apathie), waargenomen bij gebruik van HCTZ. Dubbele blokkade van het renine-angiotensine-aldosteronsysteem (RAAS) Er is bewijs dat bij gelijktijdig gebruik van ACE-remmers, angiotensine II-receptorblokkers of aliskiren het risico op hypotensie, hyperkaliëmie en een verminderde nierfunctie (inclusief acuut nierfalen) toeneemt. Dubbele blokkade van RAAS door het gecombineerde gebruik van ACE-remmers, angiotensine II-receptorblokkers of aliskiren wordt daarom niet aanbevolen (zie rubriek 4.5 en 5.1). Als behandeling met dubbele blokkade absoluut noodzakelijk wordt geacht, mag dit alleen onder supervisie van een specialist plaatsvinden en moeten de nierfunctie, elektrolyten en bloeddruk regelmatig worden gecontroleerd. ACE-remmers en angiotensine II-receptorblokkers dienen niet gelijktijdig te worden ingenomen door patiënten met diabetische nefropathie. Overige situaties met stimulatie van het renine-angiotensine-aldosteronsysteem Bij patiënten van wie de vasculaire tonus en nierfunctie voornamelijk van de activiteit van het renine-angiotensine-aldosteronsysteem afhankelijk zijn (bv. patiënten met ernstige decompensatio cordis of onderliggende nierziekte, inclusief nierarteriestenose) is de behandeling met geneesmiddelen die dit systeem beïnvloeden, geassocieerd met acute hypotensie, hyperazotemie, oligurie of, in zeldzame gevallen, acuut nierfalen (zie rubriek 4.8). Primair aldosteronisme Patiënten met primair aldosteronisme reageren in het algemeen niet op antihypertensiva die hun werking uitoefenen door inhibitie van het renine-angiotensinesysteem. Het gebruik van telmisartan/HCTZ wordt daarom niet aanbevolen. Aortaklep- en mitralisklepstenose, obstructieve hypertrofe cardiomyopathie Zoals geldt voor andere vasodilatatoren is bijzondere voorzichtigheid geboden bij patiënten die lijden aan aortaklep- of mitralisklepstenose, of obstructieve hypertrofe cardiomyopathie. Metabole en endocriene effecten Therapie met thiaziden kan de glucosetolerantie verslechteren, terwijl hypoglykemie kan voorkomen bij diabetische patiënten die behandeld worden met insuline of antidiabetica samen met telmisartan. Daarom moet worden overwogen om bij deze patiënten de bloedglucose te controleren; indien geïndiceerd, kan een aanpassing van de dosering insuline of antidiabetica noodzakelijk zijn. Een latente diabetes mellitus kan zich gedurende therapie met thiaziden manifesteren. Een verhoging van cholesterol- en triglyceridenspiegels is geassocieerd met de therapie met thiazidediuretica; bij een dosering van 12,5 mg in het geneesmiddel, zijn echter minimale of geen effecten gemeld. Hyperurikemie kan voorkomen of een uitgesproken jicht kan worden versneld bij sommige patiënten die met thiaziden worden behandeld. Verstoorde elektrolytenbalans Zoals geldt voor alle patiënten die met diuretica worden behandeld, dient periodieke bepaling van serumelektrolyten te worden uitgevoerd op geschikte tijdsintervallen. Thiaziden, inclusief hydrochloorthiazide, kunnen een verstoorde vocht- of elektrolytenbalans (inclusief hypokaliëmie, hyponatriëmie en hypochloremische alkalose) veroorzaken. Waarschuwingssignalen van een verstoorde vocht- of elektrolytenbalans zijn droge mond, dorst, asthenie, lethargie, sufheid, rusteloosheid, spierpijn of -krampen, spiervermoeidheid, hypotensie, oligurie, tachycardie en gastro-intestinale stoornissen zoals misselijkheid en braken (zie rubriek 4.8). - Hypokaliëmie Hoewel zich hypokaliëmie kan ontwikkelen bij het gebruik van thiazidediuretica, kan de gelijktijdige behandeling met telmisartan de diureticageïnduceerde hypokaliëmie verminderen. Het risico op hypokaliëmie is groter bij patiënten met levercirrose, bij patiënten met een versnelde diurese, bij patiënten met een inadequate orale inname van elektrolyten en bij patiënten die gelijktijdig worden behandeld met corticosteroïden of adrenocorticotroop hormoon (ACTH) (zie rubriek 4.5). - Hyperkaliëmie Omgekeerd, vanwege antagonisme van angiotensine II (AT1)-receptoren door het bestanddeel telmisartan in het geneesmiddel, kan hyperkaliëmie optreden. Hoewel klinisch significante hyperkaliëmie niet is gedocumenteerd voor telmisartan/HCTZ, zijn onder andere nierinsufficiëntie en/of hartfalen en diabetes mellitus risicofactoren voor de ontwikkeling van hyperkaliëmie. Kaliumsparende diuretica, kaliumsupplementen of kaliumbevattende zoutvervangers dienen met voorzichtigheid gelijktijdig te worden gebruikt met telmisartan/HCTZ (zie rubriek 4.5). - Hypochloremische alkalose Chloridedeficiëntie is doorgaans mild en vereist normaliter geen behandeling. - Hypercalciëmie Thiaziden kunnen de urinaire calciumexcretie verminderen en een intermitterende en lichte stijging van het serumcalcium veroorzaken in afwezigheid van bekende stoornissen in het calciummetabolisme. Een kenmerkende hypercalciëmie kan wijzen op een verborgen hyperparathyroïdie. De behandeling met thiaziden dient te worden gestaakt vóór het uitvoeren van onderzoek op de bijschildklierfunctie. - Hypomagnesiëmie Voor thiaziden is aangetoond dat zij de urinaire excretie van magnesium verhogen, wat kan resulteren in hypomagnesiëmie (zie rubriek 4.5). Etnische verschillen Zoals bij alle andere angiotensine II-receptorblokkers is telmisartan duidelijk minder effectief in het verlagen van de bloeddruk bij personen van Afrikaanse afkomst dan bij personen die niet van Afrikaanse afkomst zijn. Dit kan komen door hogere prevalentie van lage renineconcentraties bij personen van Afrikaanse afkomst met een te hoge bloeddruk. Ischemische hartaandoening Zoals geldt voor alle antihypertensieve middelen kan een grote daling in de bloeddruk bij patiënten met ischemische cardiopathie of ischemische cardiovasculaire aandoeningen resulteren in een myocardinfarct of een beroerte. Algemeen Overgevoeligheidsreacties op HCTZ kunnen optreden bij patiënten met of zonder voorgeschiedenis van allergie of bronchiaal astma, maar zijn waarschijnlijker bij patiënten met deze voorgeschiedenis. Exacerbatie of activering van een systemische lupus erythematodes is gemeld bij het gebruik van thiazidediuretica, waaronder HCTZ. Er zijn gevallen van fotosensibiliteitsreacties gerapporteerd bij gebruik van thiazidediuretica (zie rubriek 4.8). Als zich een fotosensibiliteitsreactie voordoet tijdens de behandeling, wordt aangeraden de behandeling te staken. Als een volgende toediening van het diureticum toch noodzakelijk wordt geacht, dan wordt aangeraden de blootgestelde huid te beschermen tegen zonlicht en kunstmatige UVA-straling. Choroïdale effusie, acute myopie en afgesloten kamerhoekglaucoom Hydrochloorthiazide, een sulfonamide, kan een idiosyncratische reactie veroorzaken, resulterend in choroïdale effusie met gezichtsvelddefect, acute tijdelijke myopie en acuut afgesloten kamerhoekglaucoom. Symptomen omvatten acuut optreden van afgenomen visuele scherpte of oculaire pijn, meestal optredend binnen uren tot weken na de start van de inname van het geneesmiddel. Onbehandeld acuut afgesloten kamerhoekglaucoom kan tot permanent verlies van het gezichtsvermogen leiden. De primaire behandeling is het zo snel mogelijk staken van de behandeling met hydrochloorthiazide. Overwogen dient te worden of snelle medische of chirurgische behandeling nodig is als de intraoculaire druk niet onder controle is. Een van de risicofactoren voor het ontwikkelen van acuut afgesloten kamerhoekglaucoom kan zijn een voorgeschiedenis van sulfonamide- of penicillineallergie. Niet-melanome huidkanker Er is een verhoogd risico op niet-melanome huidkanker (NMSC) [basaalcelcarcinoom (BCC) en plaveiselcelcarcinoom (SCC)] bij blootstelling aan een toenemende cumulatieve dosis HCTZ waargenomen bij twee epidemiologische onderzoeken op basis van het Danish National Cancer Institute (zie rubriek 4.8). De fotosensibiliserende werking van HCTZ zou kunnen werken als een mogelijk mechanisme voor NMSC. Patiënten die HCTZ innemen, moeten worden geïnformeerd over het risico op NMSC en moeten worden geadviseerd hun huid regelmatig te controleren op nieuwe laesies en verdachte huidlaesies onmiddellijk te melden. Er dienen mogelijke preventieve maatregelen zoals beperkte blootstelling aan zonlicht en uv-stralen en, in het geval van blootstelling, afdoende bescherming aan de patiënten te worden aanbevolen om het risico op huidkanker tot een minimum te beperken. Verdachte huidlaesies moeten onmiddellijk worden onderzocht, mogelijk met inbegrip van histologisch onderzoek van biopsieën. Het gebruik van HCTZ bij patiënten die eerder NMSC hebben gehad, moet mogelijk ook worden heroverwogen (zie ook rubriek 4.8). Acute respiratoire toxiciteit Er zijn zeer zeldzame ernstige gevallen van acute respiratoire toxiciteit, waaronder 'acute respiratory distress'-syndroom (ARDS), gemeld na inname van hydrochloorthiazide. Longoedeem ontwikkelt zich doorgaans binnen minuten tot uren na inname van hydrochloorthiazide. Bij aanvang omvatten de symptomen dyspneu, koorts, verslechtering van de longfunctie en hypotensie. Als de diagnose ARDS wordt vermoed, dient de behandeling met MicardisPlus te worden gestaakt en een passende behandeling te worden gegeven. Hydrochloorthiazide mag niet worden toegediend aan patiënten bij wie eerder ARDS optrad na inname van hydrochloorthiazide. Intestinaal angio-oedeem Intestinaal angio-oedeem is gemeld bij patiënten die werden behandeld met angiotensine II-receptorblokkers (zie rubriek 4.8). Bij deze patiënten deden zich buikpijn, misselijkheid, braken en diarree voor. De symptomen verdwenen na stopzetting van angiotensine II-receptorblokkers. Wanneer intestinaal angio-oedeem wordt vastgesteld, moet het gebruik van telmisartan worden gestaakt en moet gepaste monitoring plaatsvinden tot de symptomen volledig zijn verdwenen. Lactose Elke tablet bevat lactose. Patiënten met zeldzame erfelijke aandoeningen als galactose-intolerantie, algehele lactasedeficiëntie of glucose-galactose malabsorptie, dienen dit geneesmiddel niet te gebruiken. Sorbitol MicardisPlus 40 mg/12,5 mg tabletten MicardisPlus 40 mg/12,5 mg tabletten bevatten 169 mg sorbitol per tablet. MicardisPlus 80 mg/12,5 mg tabletten MicardisPlus 80 mg/12,5 mg tabletten bevatten 338 mg sorbitol per tablet. Patiënten met erfelijke fructose-intolerantie mogen dit geneesmiddel niet innemen/toegediend krijgen. Natrium Elke tablet bevat minder dan 1 mmol natrium (23 mg) per tablet, dat wil zeggen dat het in wezen 'natriumvrij' is.
Essentiële hypertensie
MicardisPlus 40 mg/12,5 mg tabletten
Elke tablet bevat 40 mg telmisartan en 12,5 mg hydrochloorthiazide.
MicardisPlus 80 mg/12,5 mg tabletten
Elke tablet bevat 80 mg telmisartan en 12,5 mg hydrochloorthiazide.
Hulpstoffen met bekend effect
MicardisPlus 40 mg/12,5 mg tabletten
Elke tablet bevat 112 mg lactosemonohydraat, overeenkomend met 107 mg watervrije lactose.
Elke tablet bevat 169 mg sorbitol (E420).
MicardisPlus 80 mg/12,5 mg tabletten
Elke tablet bevat 112 mg lactosemonohydraat, overeenkomend met 107 mg watervrije lactose.
Elke tablet bevat 338 mg sorbitol (E420).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
4.5 Interacties met andere geneesmiddelen en andere vormen van interactie Lithium Reversibele verhogingen van serumlithiumconcentraties en toxiciteit zijn gemeld gedurende gelijktijdige toediening van lithium en angiotensin converting enzyme (ACE)-remmers. Zeldzame gevallen zijn ook gemeld met angiotensine II-receptorblokkers (inclusief telmisartan/HCTZ). Gelijktijdige toediening van lithium en telmisartan/HCTZ wordt niet aangeraden (zie rubriek 4.4). Indien deze combinatie noodzakelijk blijkt, wordt aangeraden de serumlithiumspiegel nauwlettend te volgen gedurende het gelijktijdige gebruik. Geneesmiddelen die worden geassocieerd met kaliumverlies en hypokaliëmie (bv. andere kaliuretische diuretica, laxantia, corticosteroïden, ACTH, amfotericine, carbenoxolon, penicilline G, salicylzuur en zijn derivaten) Indien deze middelen gelijktijdig met de combinatie van HCTZ-telmisartan worden voorgeschreven, wordt controle van de kaliumspiegels in plasma aanbevolen. Deze geneesmiddelen kunnen het effect van HCTZ op het serumkalium versterken (zie rubriek 4.4). Jodiumhoudende contrastmiddelen In geval van dehydratie veroorzaakt door diuretica bestaat er een verhoogd risico op acuut functioneel nierfalen, in het bijzonder tijdens gebruik van hoge doses jodiumhoudende contrastmiddelen. Rehydratie vóór toediening van het jodiumhoudende contrastmiddel is vereist. Geneesmiddelen die het serumkalium kunnen verhogen of hyperkaliëmie kunnen induceren (bv. ACE-remmers, kaliumsparende diuretica, kaliumsupplementen, zoutvervangers die kalium bevatten, cyclosporine of andere geneesmiddelen zoals heparinenatrium). Indien deze geneesmiddelen met de combinatie van HCTZ-telmisartan moeten worden voorgeschreven, wordt controle van de kaliumspiegels in plasma aanbevolen. Gebaseerd op de ervaring met het gebruik van andere geneesmiddelen die het renine-angiotensinesysteem remmen, kan het gelijktijdig gebruik van de bovengenoemde geneesmiddelen leiden tot verhogingen in het serumkalium en wordt daarom niet aangeraden (zie rubriek 4.4). Geneesmiddelen die worden beïnvloed door stoornissen in het serumkalium Periodieke controle van het serumkalium en ECG wordt aanbevolen wanneer telmisartan/HCTZ wordt toegediend met geneesmiddelen die worden beïnvloed door stoornissen in het serumkalium (bv. digitalisglycosiden, antiaritmica) en de volgende geneesmiddelen die torsade de pointes induceren (waaronder enkele antiaritmica), omdat hypokaliëmie een factor is die kan leiden tot torsade de pointes. - klasse Ia-antiaritmica (bv. kinidine, hydrokinidine, disopyramide) - klasse III-antiaritmica (bv. amiodaron, sotalol, dofelitide, ibutilide) - enkele antipsychotica (bv. thioridazine, chloorpromazine, levomepromazine, trifluoperazine cyamemazine, sulpiride, sultopride, amisulpride, tiapride, pimozide, haloperidol, droperidol) - overige (bv. bepridil, cisapride, difemanil, erytromycine i.v., halofantrine, mizolastine, pentamidine, sparfloxacine, terfenadine, vincamine i.v.) Digitalisglycosiden Thiazidegeïnduceerde hypokaliëmie of hypomagnesiëmie werken het optreden van digitalisgeïnduceerde aritmie in de hand (zie rubriek 4.4). Digoxine Wanneer telmisartan gelijktijdig werd toegediend met digoxine, werd een mediane toename van de digoxinepiekplasmaconcentratie (49%) en -dalconcentratie (20%) waargenomen. Bij het initiëren, het aanpassen en het stoppen van telmisartan dient de digoxinespiegel gecontroleerd te worden, om de spiegel binnen het therapeutisch bereik te houden. Andere antihypertensiva Telmisartan kan het hypotensieve effect van andere antihypertensieve middelen vergroten. De gegevens uit klinische studies laten zien dat dubbele blokkade van het renine-angiotensine-aldosteronsysteem (RAAS) bij het gecombineerde gebruik van ACE-remmers, angiotensine II-receptorblokkers en aliskiren in verband wordt gebracht met een hogere frequentie van bijwerkingen zoals hypotensie, hyperkaliëmie en een verminderde nierfunctie (inclusief acuut nierfalen) in vergelijking met het gebruik van een enkel geneesmiddel dat op het RAAS werkt (zie rubrieken 4.3, 4.4 en 5.1). Antidiabetica (oraal en insuline) Dosisaanpassing van het antidiabeticum kan noodzakelijk zijn (zie rubriek 4.4). Metformine Metformine dient met voorzichtigheid te worden gebruikt: risico op melkzuuracidose geïnduceerd door mogelijk functioneel nierfalen bij HCTZ. Colestyramine- en colestipolharsen De absorptie van HCTZ verslechtert in de aanwezigheid van anionuitwisselingsharsen. Niet-steroïde anti-inflammatoire geneesmiddelen NSAID's (bv. acetylsalicylzuur bij anti-inflammatoire dosisregimes, COX-2-remmers en niet-selectieve NSAID's) kunnen de diuretische, natriuretische en antihypertensieve effecten van thiazidediuretica en de antihypertensieve effecten van angiotensine II-receptorblokkers verminderen. Bij sommige patiënten met een verminderde nierfunctie (bv. gedehydreerde patiënten of oudere patiënten met een verminderde nierfunctie) kan het gelijktijdig toedienen van angiotensine II-receptorblokkers en middelen die cyclo-oxygenase remmen, leiden tot een verdere verslechtering van de nierfunctie, inclusief mogelijk acuut nierfalen, dat meestal omkeerbaar is. Daarom dient de combinatie voorzichtig te worden toegediend, vooral bij ouderen. Patiënten moeten voldoende gehydrateerd zijn en het monitoren van de nierfunctie na aanvang van de gelijktijdige therapie, en vervolgens periodiek, dient overwogen te worden. In één studie leidde de gelijktijdige toediening van telmisartan en ramipril tot een toename tot 2,5 maal van de AUC0-24 en Cmax van ramipril en ramiprilaat. De klinische relevantie van deze waarneming is niet bekend. Bloeddrukverhogende amines (bv. noradrenaline) Het effect van bloeddrukverhogende amines is mogelijk verminderd. Niet-depolariserende skeletspierrelaxantia (bv. tubocurarine) Het effect van niet-depolariserende skeletspierrelaxantia kan worden versterkt door HCTZ. Geneesmiddelen gebruikt bij de behandeling van jicht (bv. probenecide, sulfinpyrazon en allopurinol) Dosisaanpassing van uricosurica kan noodzakelijk zijn, aangezien HCTZ de serumurinezuurspiegels kan verhogen. Verhoging van de dosis probenecide of sulfinpyrazon kan noodzakelijk zijn. Gelijktijdige toediening van thiazide kan de incidentie van overgevoeligheidsreacties op allopurinol verhogen. Calciumzouten Thiazidediuretica kunnen de serumcalciumspiegels verhogen door een verminderde excretie. Indien calciumsupplementen of calciumsparende geneesmiddelen (bv. vitamine D-therapie) moeten worden voorgeschreven, dienen de serumcalciumspiegels te worden gecontroleerd en dient de calciumdosis dienovereenkomstig te worden aangepast. Bètablokkers en diazoxide Het hyperglykemisch effect van bètablokkers en diazoxide kan door thiaziden worden versterkt. Anticholinergica (bv. atropine, biperideen) kunnen de biologische beschikbaarheid van thiazideachtige diuretica verhogen door vermindering van de gastro-intestinale motiliteit en de maagledigingssnelheid. Amantadine Thiaziden kunnen het risico op bijwerkingen veroorzaakt door amantadine vergroten. Cytotoxische geneesmiddelen (bv. cyclofosfamide, methotrexaat) Thiaziden kunnen de renale excretie van cytotoxische geneesmiddelen verminderen en hun myelosuppressieve effecten versterken. Gebaseerd op hun farmacologische eigenschappen is te verwachten dat de volgende geneesmiddelen het hypotensieve effect van alle antihypertensiva, inclusief telmisartan, versterken: baclofen, amifostine. Verder kan orthostatische hypotensie versterkt worden door alcohol, barbituraten, narcotica of antidepressiva.
Samenvatting van het veiligheidsprofiel De vaakst gemelde bijwerking is duizeligheid. Ernstig angio-oedeem komt in zeldzame gevallen voor (≥ 1/10.000, < 1/1.000). De totale incidentie van bijwerkingen die zijn gemeld bij telmisartan/HCTZ was vergelijkbaar met die van telmisartan alleen, in gerandomiseerde gecontroleerde studies met 1.471 gerandomiseerde patiënten die werden behandeld met telmisartan en HCTZ (835) of alleen met telmisartan (636). Voor de bijwerkingen werd geen dosisafhankelijkheid vastgesteld en er werd geen correlatie gezien met geslacht, leeftijd of ras van de patiënten. Lijst van de bijwerkingen in tabelvorm De bijwerkingen gemeld in alle klinische studies en die vaker (p ≤ 0,05) voorkwamen bij telmisartan en HCTZ dan bij placebo zijn hieronder weergegeven volgens systeem/orgaanklasse. Bijwerkingen waarvan bekend is dat ze optreden bij afzonderlijk gebruik van de bestanddelen maar die niet werden gezien in klinische studies, kunnen voorkomen tijdens de behandeling met telmisartan/HCTZ. Bijwerkingen die eerder zijn gemeld met een van de afzonderlijke bestanddelen, kunnen mogelijke bijwerkingen van MicardisPlus zijn, zelfs als deze niet zijn waargenomen tijdens klinische studies met dit product. De bijwerkingen zijn geclassificeerd met de frequentieaanduidingen aan de hand van de volgende indeling: zeer vaak (≥ 1/10); vaak (≥ 1/100, < 1/10); soms (≥ 1/1.000, < 1/100); zelden (≥ 1/10.000, < 1/1.000); zeer zelden (< 1/10.000), niet bekend (kan met de beschikbare gegevens niet worden bepaald). Binnen elke frequentiegroep worden bijwerkingen in afnemende mate van ernst genoemd.
Tabel 1: Lijst van bijwerkingen in tabelvorm (MedDRA) van placebogecontroleerde onderzoeken en postmarketingervaring
Systeem/orgaanklasse volgens MedDRA - Bijwerking - Frequentie MicardisPlus - Telmisartan - Hydrochloorthiazide
Infecties en parasitaire aandoeningen Sepsis waaronder met fatale afloop - zelden - - zelden Bronchitis - zelden - - Faryngitis - zelden - - Sinusitis - zelden - - Bovenste-luchtweginfectie - soms - - Urineweginfectie - soms - - Cystitis - soms - -
Neoplasmata, benigne, maligne en niet-gespecificeerd (inclusief cysten en poliepen) Niet-melanome huidkanker (basaalcelcarcinoom en plaveiselcelcarcinoom) - - - niet bekend
Bloed- en lymfestelselaandoeningen Anemie - soms - - Eosinofilie - zelden - - Trombocytopenie - zelden - zelden Trombocytopenische purpura - - - zelden Aplastische anemie - - - niet bekend Hemolytische anemie - - - zeer zelden Beenmergfalen - - - zeer zelden Leukopenie - - - zeer zelden Agranulocytose - - - zeer zelden
Immuunsystemaandoeningen Anafylactische reactie - zelden - - Overgevoeligheid - zelden - zeer zelden
Voedings- en stofwisselingsstoornissen Hypokaliëmie - soms - zeer vaak Hyperurikemie - zelden - vaak Hyponatriëmie - zelden - zelden - vaak Hyperkaliëmie - - soms - Hypoglykemie (bij diabetische patiënten) - - zelden - Hypomagnesiëmie - - vaak - Hypercalciëmie - - zelden - Hypochloremische alkalose - - zeer zelden - Verminderde eetlust - - vaak - Hyperlipidemie - - zeer vaak - Hyperglykemie - - zelden - Diabetes mellitus, inadequate beheersing - - zelden -
Psychische stoornissen Angst - soms - zelden - Depressie - zelden - soms - zelden Slapeloosheid - zelden - soms - Slaapstoornissen - zelden - zelden -
Zenuwstelselaandoeningen Duizeligheid - vaak - zelden - Syncope - soms - soms - Paresthesie - soms - zelden - Slaperigheid - zelden - -
Oogaandoeningen Gezichtsvermogen afgenomen - zelden - zelden - zelden Gezichtsvermogen wazig - zelden - - Acuut afgesloten-kamerhoekglaucoom - - - niet bekend Choroidale effusie - - - niet bekend
Evenwichtsorgaan- en ooraandoeningen Vertigo - soms - soms -
Hartaandoeningen Tachycardie - soms - zelden - Aritmieën - soms - zelden - Bradycardie - soms - -
Bloedvataandoeningen Hypotensie - soms - soms - Orthostatische hypotensie - soms - soms - vaak Necrotiserende vasculitis - - - zeer zelden
Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen Dyspneu - soms - soms - Respiratoire stress - zelden - zeer zelden Pneumonitis - zelden - zeer zelden Pulmonaal oedeem - zelden - zeer zelden Hoesten - soms - -
Interstitiële longziekte - - zeer zelden1,2 -
Acuut ademhalingsnoodsyndroom (ARDS) (zie rubriek 4.4) - - - zeer zelden
Maagdarmstelselaandoeningen Diarrree - soms - soms - vaak Droge mond - soms - zelden - Flatulentie - soms - soms - Buikpijn - zelden - soms - Constipatie - zelden - zelden - Dyspepsie - zelden - soms - Braken - zelden - soms - vaak Gastritis - zelden - - Maagklachten - zelden - zelden - Misselijkheid - - vaak - Pancreatitis - - zeer zelden -
Lever- en galaandoeningen Afwijkende leverfunctie/leveraandoening - zelden2 - zelden2 - Geelzucht - - zelden - Cholestase - - zelden -
Huid- en onderhuidaandoeningen Angio-oedeem (ook met fatale afloop) - zelden - zelden - Erytheem - zelden - zelden - Pruritus - zelden - soms - Rash - zelden - soms - vaak Hyperhidrose - zelden - soms - Urticaria - zelden - zelden - vaak Eczeem - - zelden - Geneesmiddeleneruptie - - zelden -
Toxische huideruptie - - zelden - Lupusachtig syndroom - - zeer zelden - Fotosensitiviteitsreactie - - zelden - Toxische epidermale necrolyse - - zeer zelden - Erythema multiforme - - niet bekend -
Skeletspierstelsel- en bindweefselaandoeningen Rugpijn - soms - soms - Spierspasmen (beenkrampen) - soms - soms - niet bekend Myalgie - soms - soms - Artralgie - zelden - zelden - Pijn in extremiteit (beenpijn) - zelden - zelden - Peespijn (tendinitisachtige symptomen) - - zelden - Gegeneraliseerde lupus erythematosus - zelden1 - zeer zelden -
Nier- en urinewegaandoeningen Nierfunctie verminderd - soms - niet bekend Acuut nierfalen - soms - soms - Glucosurie - - zelden -
Voortplantingsstelsel- en borstaandoeningen Erectiele disfunctie - soms - vaak
Algemene aandoeningen en toedieningsplaatsstoornissen Borstkaspijn - soms - soms - Influenza-achtige ziekte - zelden - zelden - Pijn - zelden - - Asthenie (zwakte) - soms - niet bekend Pyrexie - - niet bekend
Onderzoeken Bloed urinezuur verhoogd - soms - zelden Bloed creatinine verhoogd - zelden - soms Bloed creatinefosfokinase verhoogd - zelden - zelden Leverenzym verhoogd - zelden - zelden Hemoglobine verlaagd - zelden - -
Beschrijving van geselecteerde bijwerkingen Afwijkende leverfunctie/leveraandoening De meeste gevallen van afwijkende leverfunctie/leveraandoening tijdens postmarketingervaring van telmisartan traden op bij patiënten van Japanse origine. Patiënten van Japanse origine hebben een grotere kans op het krijgen van deze bijwerkingen. Sepsis In het PRoFESS-onderzoek, werd een verhoogde incidentie van sepsis waargenomen met telmisartan vergeleken met placebo. Dit kan berusten op toeval of gerelateerd zijn aan een tot nu toe onbekend mechanisme (zie rubriek 5.1).
Bijwerkingen waarvan bekend is dat ze optreden bij afzonderlijk gebruik van de bestanddelen maar die niet werden gezien in klinische studies, kunnen voorkomen tijdens de behandeling met telmisartan/HCTZ. Bijwerkingen die eerder zijn gemeld met een van de afzonderlijke bestanddelen, kunnen mogelijke bijwerkingen van MicardisPlus zijn, zelfs als deze niet zijn waargenomen tijdens klinische studies met dit product.
De bijwerkingen zijn geclassificeerd met de frequentieaanduidingen aan de hand van de volgende indeling: zeer vaak (≥ 1/10); vaak (≥ 1/100, < 1/10); soms (≥ 1/1.000, < 1/100); zelden (≥ 1/10.000, < 1/1.000); zeer zelden (< 1/10.000), niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Binnen elke frequentiegroep worden bijwerkingen in afnemende mate van ernst genoemd.
• Overgevoeligheid voor de werkzame bestanddelen of voor één van de in "Samenstelling" vermelde hulpstoffen.
• Overgevoeligheid voor andere sulfonamide afgeleide stoffen (aangezien hydrochloorthiazide een van sulfonamiden afgeleid geneesmiddel is).
• Tweede en derde trimester van de zwangerschap .
• Cholestasis en galwegobstructies.
• Ernstige leverinsufficiëntie.
• Ernstige nierinsufficiëntie (creatinineklaring < 30 ml/min).
• Refractaire hypokaliëmie, hypercalciëmie.
Het gelijktijdig gebruik MicardisPlus met aliskiren-bevattende geneesmiddelen is gecontra-indiceerd bij patiënten met diabetes mellitus of nierinsufficiëntie (GFR < 60 ml/min/1,73 m2) .
Zwangerschap Het gebruik van angiotensine II-receptorblokkers wordt niet aanbevolen tijdens het eerste trimester van de zwangerschap (zie rubriek 4.4). Het gebruik van angiotensine II-receptorblokkers is gecontra-indiceerd tijdens het tweede en derde trimester van de zwangerschap (zie rubriek 4.3 en 4.4). Er zijn geen toereikende gegevens over het gebruik van telmisartan/HCTZ bij zwangere vrouwen. Uit dieronderzoek is reproductietoxiciteit gebleken (zie rubriek 5.3). Er kunnen geen duidelijke conclusies getrokken worden uit epidemiologisch bewijs over het risico van teratogeniciteit na blootstelling aan ACE-remmers tijdens het eerste trimester van de zwangerschap; een kleine toename in het risico kan echter niet worden uitgesloten. Hoewel er geen gecontroleerde epidemiologische gegevens zijn over het risico van angiotensine II-receptorblokkers kan het risico vergelijkbaar zijn bij deze klasse van geneesmiddelen. Patiënten die een zwangerschap plannen, moeten omgezet worden op een alternatieve antihypertensieve therapie met een bekend veiligheidsprofiel voor gebruik tijdens de zwangerschap, tenzij het voortzetten van de angiotensine II-receptorblokkertherapie noodzakelijk wordt geacht. Als zwangerschap wordt vastgesteld, dient de behandeling met angiotensine II-receptorblokkers onmiddellijk te worden gestaakt, en moet, indien nodig, worden begonnen met een alternatieve therapie. Het is bekend dat blootstelling aan angiotensine II-receptorblokkertherapie gedurende het tweede en derde trimester bij de mens foetale toxiciteit (verslechterde nierfunctie, oligohydramnie, achterstand in schedelverharding) en neonatale toxiciteit (nierfalen, hypotensie, hyperkaliëmie) kan induceren (zie rubriek 5.3). Als blootstelling aan angiotensine II-receptorblokkers vanaf het tweede trimester van de zwangerschap heeft plaatsgevonden, wordt een echoscopie van de nierfunctie en de schedel aanbevolen. Zuigelingen van wie de moeder angiotensine II-receptorblokkers heeft gebruikt, dienen nauwgezet gecontroleerd te worden op hypotensie (zie rubriek 4.3 en 4.4). Er is beperkte ervaring met het gebruik van HCTZ tijdens de zwangerschap, met name in het eerste trimester. Dieronderzoek heeft onvoldoende gegevens opgeleverd. Hydrochloorthiazide passeert de placenta. Op basis van het farmacologische werkingsmechanisme van HCTZ kan het gebruik hiervan tijdens het tweede en derde trimester de foetoplacentaire perfusie verstoren en leiden tot foetale en neonatale effecten zoals icterus, verstoring van de elektrolytenbalans en trombocytopenie. Hydrochloorthiazide mag niet worden gebruikt voor zwangerschapsoedeem, zwangerschapshypertensie of pre-eclampsie, omdat dit het risico op verminderd plasmavolume en placentaire hypoperfusie oplevert, terwijl het geen positieve invloed op het beloop van de ziekte heeft. Hydrochloorthiazide mag niet worden gebruikt voor essentiële hypertensie bij zwangere vrouwen, behalve in het zeldzame geval dat er geen andere behandeling mogelijk is. Borstvoeding Omdat er geen informatie beschikbaar is over het gebruik van telmisartan/HCTZ bij het geven van borstvoeding, wordt telmisartan/HCTZ niet aangeraden. Alternatieve behandelingen met beter bekende veiligheidsprofielen verdienen de voorkeur, vooral bij het geven van borstvoeding aan pasgeboren of prematuur geboren zuigelingen. Hydrochloorthiazide wordt in kleine hoeveelheden in de moedermelk uitgescheiden. Hoge doses thiaziden kunnen door sterke diurese de melkproductie remmen. Het gebruik van telmisartan/HCTZ tijdens het geven van borstvoeding wordt niet aanbevolen. Als telmisartan/HCTZ gebruikt wordt tijdens het geven van borstvoeding dient de dosis zo laag mogelijk te worden gehouden. Vruchtbaarheid Er is geen onderzoek uitgevoerd naar de vruchtbaarheid bij mensen met de vaste dosiscombinatie of de afzonderlijke bestanddelen. In preklinische studies werd geen effect van telmisartan en HCTZ op de mannelijke en vrouwelijke vruchtbaarheid waargenomen.
Volwassenen vanaf 18 jaar
Toedieningswijze
| CNK | 1732130 |
|---|---|
| Organisaties | Boehringer Ingelheim |
| Merken | Boehringer |
| Breedte | 109 mm |
| Lengte | 116 mm |
| Diepte | 71 mm |
| Hoeveelheid verpakking | 98 |
| Actieve ingrediënten | hydrochloorthiazide, telmisartan |
| Behoud | Kamertemperatuur (15°C - 25°C) |